Miniaturisé et communiquant ses données sans fil, l’implant intracérébral développé par Neuralink, la société de neurotechnologie du fantasque milliardaire, intrigue les chercheurs. Pourrait-il avoir bientôt des applications cliniques intéressantes ? Nous avons demandé son avis à un spécialiste de l’épilepsie.
Début avril, une vidéo a fait le tour de la Toile. On y voyait Pager, un macaque de 9 ans, jouant au jeu Pong par la pensée grâce à l’implant cérébral développé par Neuralink, l’entreprise fondée par l’entrepreneur Elon Musk (Tesla, SpaceX). Spectaculaire… mais pas franchement révolutionnaire. En effet, en 2016, des chercheurs du Duke Center for Neuroengineering de l’université de Duke (Caroline du Nord) étaient déjà parvenus à ce que des primates commandent une chaise roulante par la pensée, et ce avec un système sans fil. Alors, cette nouvelle expérience menée par les équipes du fantasque milliardaire mérite-t-elle qu’on s’y arrête ? Nous avons posé la question au Dr Julien Jung, neurologue et chercheur au CRNL, spécialiste de l’épilepsie.
Une puce de la taille d’une grosse pièce de monnaie.
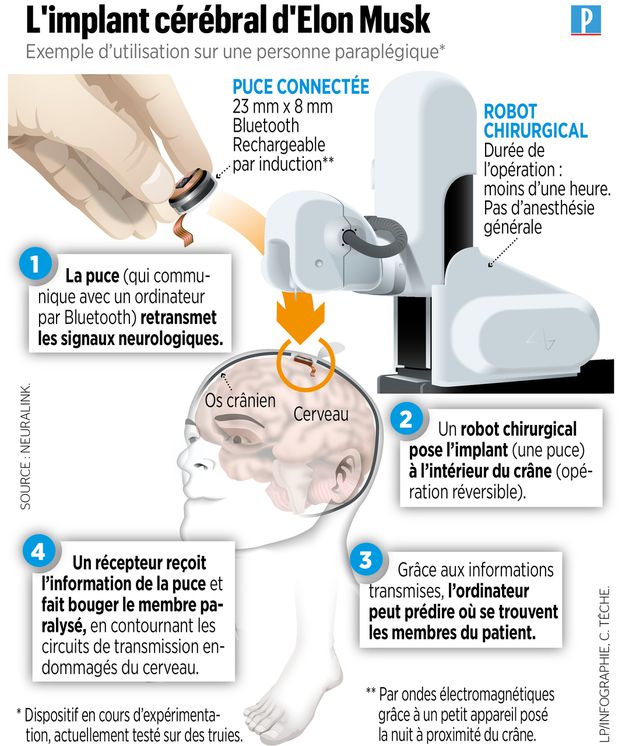
Pour commencer, intéressons-nous à l’implant de Neuralink. Son principal atout est sa taille. La puce mesure 23 mm de diamètre et 8mm d’épaisseur. Elle est reliée à un réseau de fils extrêmement fins (20 fois plus qu’un cheveu), chacun possédant 1024 électrodes permettant d’enregistrer l’activité cérébrale. Les données acquises sont ensuite transmises par une technologie sans fil (Bluetooth) à un ordinateur. La puce serait alimentée par une batterie rechargeable par induction. Autre innovation : la puce et ses électrodes seraient implantée par un robot chirurgien. Selon Elon Musk, l’opération réalisée sans anesthésie générale ne prendrait pas plus d’une heure.
A ce jour, le dispositif aurait été implanté avec succès chez des cochons et des singes et devrait l’être prochainement chez l’homme. Le problème avec Neuralink est que les informations « relèvent plus de l’effort de communication que de l’exposé scientifique », comme le souligne Jérémie Mattout, chercheur au CRNL. Dans une interview au Parisien, ce spécialiste des interfaces cerveau-machine espére que ces avancées « feront l’objet de publications détaillées, revues par experts indépendants, pour que l’on puisse réellement en apprécier la portée par rapport à ce qui se fait par ailleurs dans différents laboratoires publics de par le monde ».
> Vidéo de la conférence de presse d’Elon Musk en août 2020.
A quoi pourrait servir cet implant cérébral ? A court terme, Elon Musk affirme qu’il permettra, par exemple, à des personnes avec des lésions de la moelle épinière de commander un exosquelette par la pensée. Ou encore de traiter des maladies neurologiques telle que Parkinson ou l’épilepsie. A plus long terme, il promet carrément d’augmenter les capacités du cerveau humain. Grâce à ce minuscule implant, chacun serait capable de rivaliser avec le niveau de calcul d’un ordinateur, de stocker des souvenirs de façon numérique ou encore de décrypter les pensées de son voisin de table ! Laissons à Elon Musk la liberté d’imaginer les applications les plus folles des technologies qu’il finance… Et intéressons-nous aux retombées que cet implant cérébral high-tech pourrait avoir pour les patients souffrant de formes graves d’épilepsie.
A ce jour, les implants intracérébraux ne sont utilisés que dans de rares cas de patients épileptiques pharmacorésistants.
Aujourd’hui les implants intracérébraux permettant de mesurer l’activité cérébrale sont surtout utilisés dans le domaine de la recherche fondamentale, principalement chez des rongeurs ou des primates non humains. Dans le domaine clinique chez l’humain, ils ne sont utilisés que dans de rares cas de patients épileptiques pharmacorésistants. « Dans ce cas de figure, explique Julien Jung, on cherche à réséquer [enlever] le ou les foyers épileptiques sans léser de zones associées à des fonctions essentielles du cerveau. » Pour cela, les spécialistes utilisent des électrodes appelées sEEG, qui permettent d’enregistrer des populations de neurones afin de confirmer la localisation de ces foyers épileptiques. « Depuis une dizaine d’années maintenant, ajoute le neurologue, on peut coupler ces sEEG à des enregistrements dits de microcontact, permettant d’enregistrer l’activité unitaire des neurones. Ces enregistrements n’ont toutefois aucune utilité clinique à ce jour et servent uniquement la recherche fondamentale. » En effet, on ne dispose aujourd’hui d’aucun marqueur parfait de la zone à réséquer dans le cas de l’épilepsie. C’est pourquoi on enlève encore des zones très larges.
> A ce sujet, lire notre article « Chirurgie de l’épilepsie : une solution pour les patients résistants aux médicaments ».
Avec son implantation ciblée, l’implant développé par Neuralink permettrait, si les promesses sont tenues, d’appréciables avancées sur le plan technique. Deux points retiennent en particulier l’attention de Julien Jung. La taille de l’implant, d’abord : « La miniaturisation des électrodes permettrait de minimiser les dommages vasculaires associés à l’implantation. » Deuxième point intéressant : la transmission des données sans fil. Aujourd’hui, les patients implantés ont des vis fixées dans le crâne et des câbles nécessitant un branchement pour récolter les données. Cela représente une contrainte pour le patient et augmente en même temps le risque d’infection à cause du passage du dispositif à travers le scalp. « Une implantation intracérébrale, via la technologie Bluetooth, serait plus écologique pour le patient. »
L’implant de Neuralink aurait plus d’avenir dans le domaine des interfaces cerveau-machine.
En l’état actuel des connaissances, l’utilité clinique de l’implant Neuralink dans le champ de l’épilepsie n’est donc pas avérée. « Certes, le fait d’enregistrer des neurones unitaires pourrait permettre de mieux cibler la zone à opérer, nuance Julien Jung. Mais cela reste à démontrer. » Le neurologue lui voit plus d’avenir « dans le domaine de la recherche, dans celui des pathologies avec une cible très locale ou encore dans celui des interfaces cerveau-machine ». Il cite à cet égard l’interface cerveau-machine (ICM) de nouvelle génération que vient de développer une équipe de l’université de Stanford. Dans un article récemment publié dans Nature, les chercheurs expliquent comment ils sont parvenus à décoder l’activité des circuits cérébraux dédiés à l’écriture manuscrite et ont créé une ICM qui transcrit, à un rythme deux fois plus rapide que les ICM classiques, les lettres qu’un sujet paralysé de la main visualise mentalement. « Dans ce cas, estime Julien Jung, l’implant Neuralink permettrait de s’affranchir de la contrainte des fils du dispositif et faciliterait grandement le quotidien des personnes paralysées. » Moins futuriste que le « cerveau augmenté », mais nettement plus utile…







