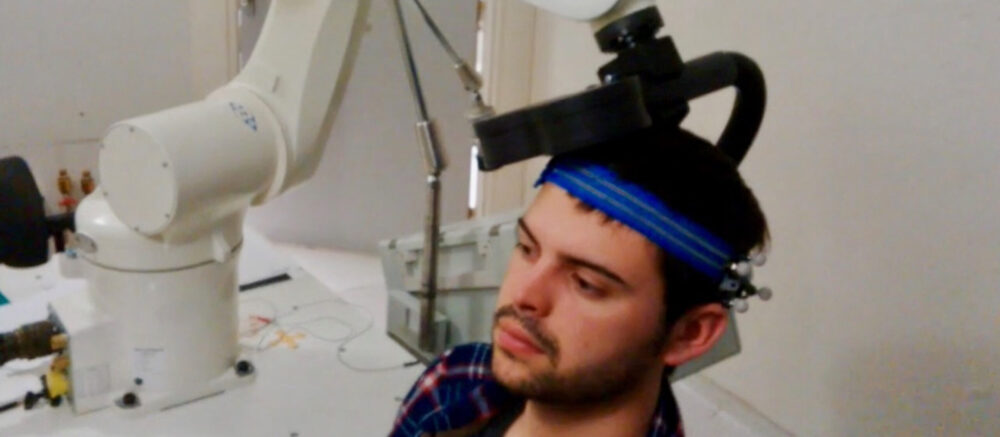
Quelles solutions proposer aux personnes atteintes de douleurs neuropathiques lorsque les traitements médicamenteux sont sans effet ? Une équipe du CRNL utilise avec succès la rTMS, une technique de stimulation du cortex cérébral via des impulsions magnétiques.
Toutes les douleurs ne se valent pas. Les plus courantes sont dues à une lésion du corps : brûlure, fracture, coupure, inflammation tissulaire… D’autres peuvent se déclencher sans raison physique apparente et provoquer des sensations tout aussi désagréables. Ceux qui en souffrent les décrivent comme une brûlure, des fourmillements, un coup de poignard ou une décharge électrique. On parle alors de douleurs neuropathiques. Ces douleurs résultent d’un dysfonctionnement du système nerveux, le plus souvent dû à une atteinte des nerfs périphériques (nerfs coupés ou arrachés, neuropathies diabétiques…), de la moelle épinière ou du cerveau (traumatisme médullaire, AVC, sclérose en plaque…). Il arrive aussi que certaines personnes ressentent de fortes douleurs à la suite d’une stimulation normalement indolore, comme un simple effleurement ou une douche. On parle alors d’allodynie.
Des antiépileptiques et des antidépresseurs contre les douleurs neuropathiques
Comment soulager ces patients douloureux ? La réponse n’est pas simple car bien souvent les antalgiques classiques ne leur apportent que peu de soulagement. La pharmacopée disponible à ce jour s’appuie majoritairement sur des antiépileptiques et des antidépresseurs, dont le principe actif permet d’atténuer le dysfonctionnement neurologique, source de ces douleurs. Néanmoins, ces traitements ont une efficacité limitée (40%) et sont souvent mal tolérés par les patients en raison d’effets secondaires importants (somnolence, vertige, trouble de l’humeur…). Cette question soulève donc un vrai problème de santé publique : on estime en effet à 5% la part de la population souffrant de douleurs neuropathiques chroniques. [1]
Face à ce manque d’efficacité, des alternatives thérapeutiques émergent depuis une vingtaine d’années. Parmi elles, la stimulation du cortex moteur primaire. C’est le Pr Tsubokawa, neurochirurgien japonais, qui a le premieren 1991, démontré qu’une stimulation des aires motrices primaires pouvait soulager en partie les douleurs neuropathiques d’origines centrales. Depuis, de nombreuses équipes, notamment à Lyon et Saint-Etienne, ont implanté avec succès des patients douloureux. Toutefois, cette technique chirurgicale, bien que moins complexe qu’une stimulation cérébrale profonde, présente au moins deux limites. La première est liée à son caractère invasif, avec les risques inhérents à toute intervention neurochirurgicale. La seconde vient du fait qu’il est difficile de savoir à l’avance si le patient répondra ou non à la stimulation. C’est pourquoi, dès la fin des années 1980, on a cherché à développer des techniques non-invasives du cortex. L’une d’elle consiste à utiliser de puissants champs magnétiques qui, s’ils sont suffisamment concentrés (loi de Faraday), permettent d’induire un champ électrique à distance. La stimulation magnétique transcrânienne (TMS) était née. Elle devient, dans les années 90, la stimulation magnétique transcrânienne répétitive (rTMS), à la suite d’une amélioration technologique permettant de produire des stimulations répétées.
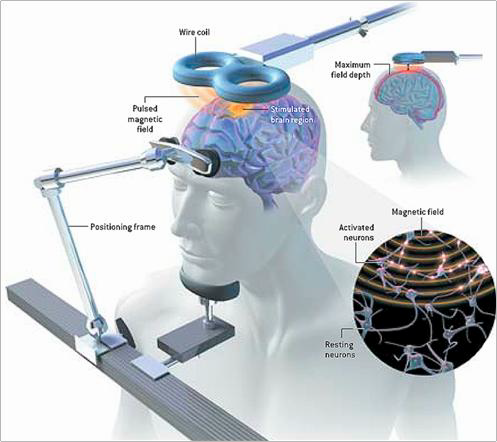
Dispositif de stimulation transcrânienne (Image : Afat).
Concrètement, comment cela fonctionne-t-il ? La stimulation magnétique produit un champ électrique d’environ 12 mV à une profondeur comprise entre 2 et 3 cm sous la sonde. On provoque alors – une fois le scalp, l’os, les méninges, le liquide céphalorachidien passés – une stimulation corticale de surface. Appliquée, par exemple, sur la zone du cortex moteur primaire alloué à la commande de la main, une stimulation suffisamment forte de rTMS provoque une contraction ponctuelle des muscles de la main. Médecins et chercheurs ont rapidement vu l’intérêt thérapeutique de cette technique de stimulation, par ailleurs indolore et dépourvue d’effets secondaires.
Au début des années 2000, de nombreuses équipes ont cherché à reproduire les résultats obtenus par stimulation électrique de surface chez des patients douloureux chroniques neuropathiques. Bien qu’un effet antalgique ait été démontré, celui-ci est souvent resté modeste et de courte durée. Malgré ces limites, la rTMS s’est révélée un excellent indicateur prédictif pour la réussite de la stimulation corticale motrice par implantation (SCM) : « A ce jour, tous les répondants à la rTMS ont aussi été répondants à la SCM », constate Benjamin Pommier, neurochirurgien à l’hôpital de Saint-Etienne.
La rTMS efficace aussi en psychiatrie
La stimulation magnétique transcrânienne répétitive (rTMS) n’est pas seulement utilisée pour soulager les douleurs neuropathiques. Elle a aussi fait ses preuves dans le domaine de la psychiatrie, notamment dans le traitement de la dépression, des addictions ou de la réhabilitation après un accident vasculaire cérébral. Récemment, une équipe de recherche française a utilisé avec succès la rTMS pour réduire les hallucinations auditives de patients schizophrènes.
Aujourd’hui, la rTMS pour le traitement des douleurs neuropathiques centrales connait un net regain d’intérêt. Celui-ci est dû à des améliorations techniques qui permettent une plus grande précision dans la localisation et la délivrance des stimulations. En particulier l’utilisation d’un système de neuronavigation basé sur l’IRM anatomique cérébral du patient. Cet outil permet de visualiser la zone à stimuler et d’y définir une cible précise et réutilisable d’une séance à l’autre.
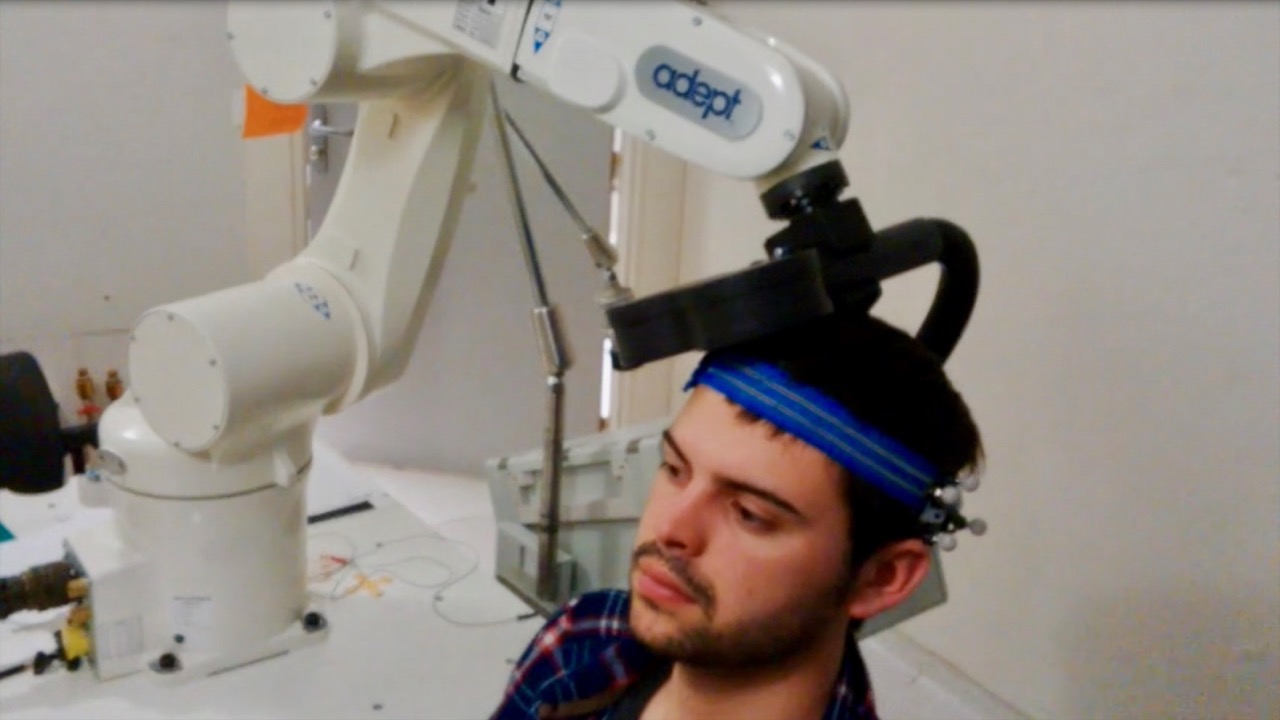
En outre, ce système de neuronavigation peut être associé à un système de bras robotique et de caméra optoélectronique 3D (photo ci-dessus). « L’intérêt de ce dispositif est de maintenir la sonde de stimulation sur la cible prédéfinie durant toute la séance, et ce malgré les mouvements fortuits de la tête du patient », explique Charles Quesada, doctorant, membre de l’équipe Neuropain de Saint-Etienne.
Des effets antalgiques après plusieurs séances
De nouvelles études ont montré l’efficacité de ce protocole contre les douleurs neuropathiques. Notamment un effet cumulatif chez 60% des patients traités après plusieurs séances espacées de 3 à 4 semaines. [2] Si l’effet antalgique de la rTMS semble en passe d’être démontré, les mécanismes sous-jacents sur lesquels reposerait cette analgésie restent en revanche encore hypothétiques. Les dernières études évoquent avec prudence d’éventuels changements d’activité dans des boucles thalamo-corticales mettant en jeu le système d’opioïdes endogènes. [3] Il a ainsi été décrit qu’après une stimulation par rTMS se produisait une diminution d’activité chez les patients répondeurs au niveau du cortex somesthésique (primaire et secondaire), de l’insula, du cortex préfrontal et du putamen. Ce phénomène laisse penser que le mécanisme antalgique résultant de la stimulation par rTMS pourrait être due à une modulation de l’activité neuronale du réseau de la douleur de manière distribuée entre ces différentes aires. [4] [5]
Bientôt une solution portative pour soulager les patients à domicile ?
Ingénieure de recherche au CRNL, Caroline Perchet travaille sur un programme permettant aux personnes souffrant de neuropathies chroniques d’agir elles-mêmes sur la douleur sans bouger de chez elles. Ce programme fait appel à une autre forme de stimulation transcrânienne, basée non sur la concentration d’un champ magnétique mais sur l’utilisation d’un courant continu, plus facile à manipuler. Après s’être familiarisés à l’hôpital avec le matériel et le dispositif, les patients peuvent se livrer à domicile à des séances d’autostimulation, néanmoins contrôlées à distance via une application. Bien qu’il soit trop tôt à ce jour pour quantifier l’efficacité de cette technique, les patients témoignent spontanément d’une amélioration sensible de leur quotidien.
Les enjeux autour de la stimulation par rTMS sont importants. D’abord sur le plan médical : cette technique permet de proposer une solution aux patients – nombreux – qui ne sont pas soulagés par les traitements médicamenteux et ceux pour qui les traitements antalgiques présentent des effets secondaires. Sur le plan économique, ensuite : une stimulation mensuelle par rTMS se substituant à un traitement médicamenteux quotidien représenterait une source d’économie pour le système de soins. Enfin, d’un point de vue scientifique, si la rTMS démontrait qu’en modulant l’activité neuronale de certaines zones du cerveau on parvient à moduler la perception douloureuse, cela ouvrirait la voie à une meilleure compréhension des mécanismes de régulation et de traitement de la douleur au niveau cérébral. ♦
Publications
> J’ai mal pour toi : fondements neuronaux et cognitifs de l’empathie
> Luis Garcia-Larrea cherche là où ça fait mal